
精彩内容
分羹400亿市场,抑酸新品获批上市
三联COPD新药上市,AZ霸主地位难撼
2款儿科新药来袭,芍麻止痉颗粒已获批
3款国产1类新药获批上市
“伟哥”焕发第二春?新剂型即将获批
又有利妥昔单抗生物类似药报产
恒瑞5个新药临床申请获承办
9个新药上市,4款国产新药接连获批
近两周(12.13-12.27)有26个报产的新药受理号有审评审批状态更新,8个受理号(5个品种)获批进口;4个受理号(4个品种)获批上市;14个受理号(11个品种)暂时未有审评结论,西地那非新剂型要来了。
表1:近两周报产新药审评审批状态更新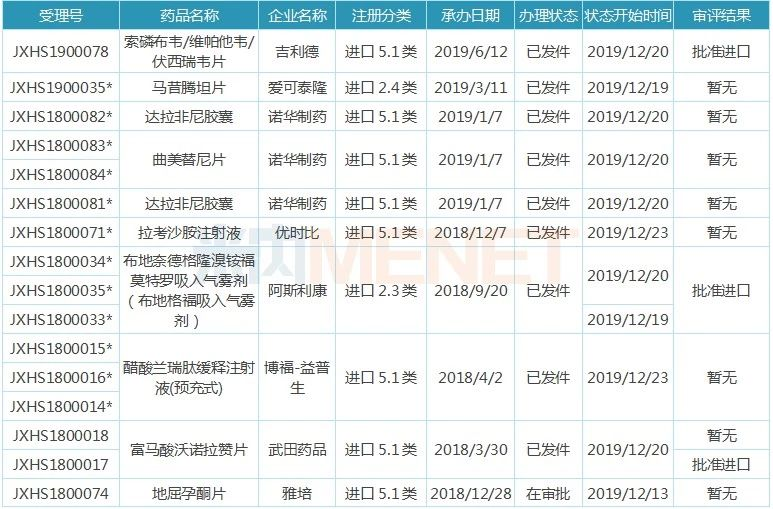
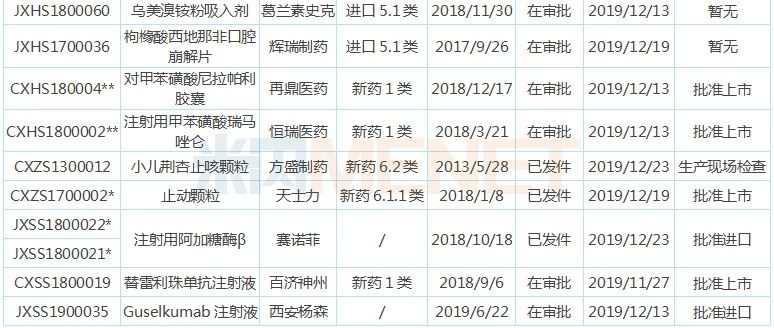
注:带*为优先审评,**为特殊审评+优先审评
5个新药获批进口,分别为吉利德的“吉四代”索磷布韦/维帕他韦/伏西瑞韦片、阿斯利康的三联COPD新药布地格福吸入气雾剂、武田的抑酸新品富马酸沃诺拉赞片、赛诺菲的罕见病用药注射用阿加糖酶β、西安杨森的临床急需药物Guselkumab注射液。
阿斯利康的布地格福吸入气雾剂是国内目前唯一采用压力定量气雾剂(pMDI)装置的三联吸入制剂,用于稳定期慢性阻塞性肺病(COPD)的长期维持治疗。研究结果显示,与双联支气管扩张剂治疗相比,布地格福吸入气雾剂能够显著降低COPD患者52%的中重度急性加重率,并延长到达首次中重度急性加重时间。同时,该药物起效快速并可持续显著改善患者肺功能,且具有良好的安全性。
米内网数据显示,目前国内治疗哮喘及慢阻肺的药物仍以单方制剂为主,TOP10品牌中有8个为外资品牌,其中阿斯利康独占3席,普米克令舒、信必可都保、博利康尼3款产品在2018年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端的销售额均超10亿元,合计销售额超过100亿元。布地格福吸入气雾剂的获批将有助于巩固阿斯利康在国内呼吸领域的主导地位。
富马酸沃诺拉赞片是武田研制的钾离子竞争性酸阻滞剂(P-CAB),于2015年2月在日本上市,用于治疗酸相关疾病。体外活性实验表明该化合物抑制质子泵的能力是兰索拉唑的400倍。目前国产注册沃诺拉赞热情高涨,申报临床的受理号已达34个,其中16个受理号(涉及8家药企)已获批临床。
2018年中国公立医疗机构终端治疗与胃酸分泌相关疾病用药市场突破400亿元,TOP10品种均为质子泵抑制剂,合计销售额近320亿元,沃诺拉赞的上市有望分一杯羹。
芍麻止痉颗粒为天士力的独家品种,具有平抑肝阳,息风止痉,清火豁痰的功效,适用于儿童期Tourette 综合征(抽动-秽语综合征)及慢性抽动障碍。临床研究结果表明,芍麻止痉颗粒疗效明确,安全性良好。
3个国产1类新药、1个儿科中成药新药获批上市,分别为再鼎的对甲苯磺酸尼拉帕利胶囊、恒瑞的麻醉剂新药注射用甲苯磺酸瑞马唑仑、百济神州的PD-1替雷利珠单抗注射液、天士力的芍麻止痉颗粒(曾用名:止动颗粒)。
对甲苯磺酸尼拉帕利胶囊是全球首个用于卵巢癌二线治疗的PARP抑制剂,2016年再鼎医药从Tesaro获得该产品在中国的独家研发与销售权,2018年10月、2019年6月相继在香港、澳门上市。米内网中国药品临床试验公示库显示,尼拉帕利在铂敏感复发卵巢癌二线维持治疗、一线维持治疗和非小细胞肺癌3个适应症已在开展III期临床。
恒瑞医药的注射用甲苯磺酸瑞马唑仑是一种短效的GABAa受体激动剂,适用于择期手术中的静脉全身麻醉。该产品结合了咪达唑仑的安全性与丙泊酚的有效性,具有起效和失效迅速、镇静作用稳定、恢复时间短等特点。
米内网数据显示,2018年中国公立医疗机构终端麻醉剂的销售额已超百亿元,同比增长12.4%。近年来住院手术量不断提升,再加上麻醉新品的带动,推动了麻醉剂市场的快速扩容。麻醉剂是恒瑞医药三大核心业务板块之一,手握七氟烷、右美托咪定和顺阿曲库铵等大品种,甲苯磺酸瑞马唑仑若获批上市,将成为公司麻醉线新的利润增长点。
13个新药上市申请获承办,又有利妥昔单抗生物类似药报产
近两周(12.13-12.27)承办的新药/进口上市申请共26个受理号(13个品种),其中8个受理号(6个品种)为国产新药上市申请,18个受理号(7个品种)为进口新药上市申请;从药物类型看,10个受理号(4个品种)为化学药,15个受理号(8个品种)为治疗用生物制品,1个受理号(1个品种)为中成药。
表2:近两周新药/进口上市申请承办情况
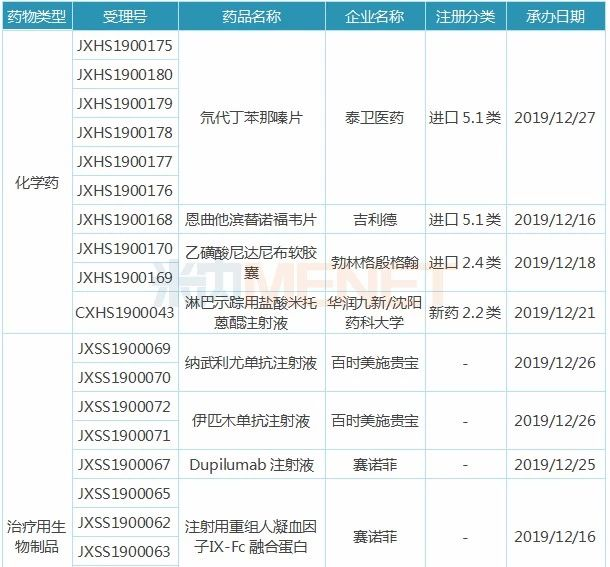

神州细胞工程的利珀妥单抗注射液为利妥昔单抗生物类似药,米内网数据显示,2018年中国公立医疗机构终端利妥昔单抗注射液销售额为35.35亿元。首个利妥昔单抗生物类似药于2019年2月获批上市,花落复宏汉霖,神州细胞工程是继信达后又一家提交利妥昔单抗生物类似药上市申请的企业,此外华兰基因、喜康生物、正大天晴、海正药业等企业的产品处于临床III期,未来将陆续申报上市。
34个新药临床申请获承办,恒瑞独占5席
近两周(12.13-12.27)承办的新药/进口临床申请共49个受理号(34个品种),其中32个受理号(22个品种)为国产新药临床申请,17个受理号(12个品种)为进口新药临床申请;从药物类型看,30个受理号(18个品种)为化学药,18个受理号(15个品种)为治疗用生物制品,1个受理号(1个品种)为中成药。
虽然申报上市的国产新药比进口新药少,但申报临床的国产新药比进口新药多了近一倍,可见国内企业正在往创新发展转型,未来将会有越来越多的国产新药申报上市。
表3:近两周新药/进口临床申请承办情况
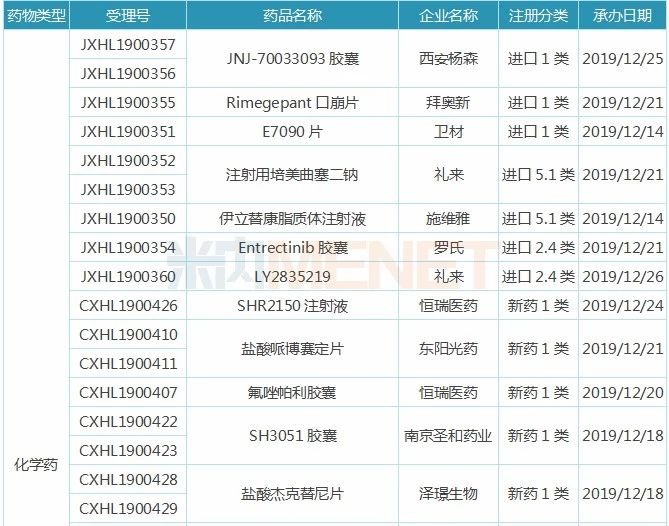
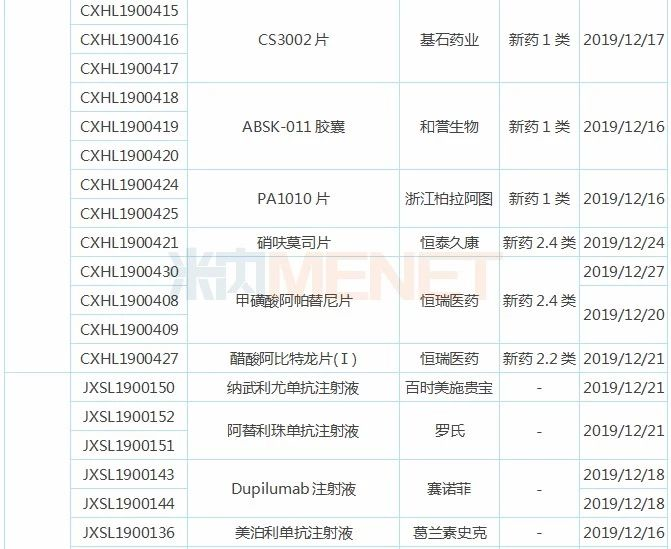
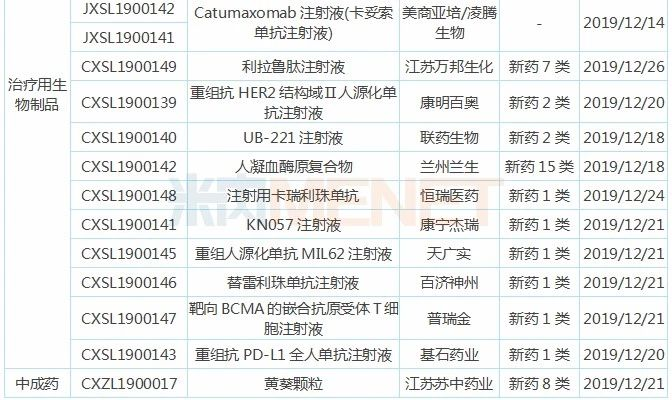
近两周恒瑞医药有7个受理号(5个品种)临床申请获得CDE承办受理,SHR2150是一种Toll样受体7(TLR-7)抑制剂,拟用于治疗晚期恶性肿瘤,其胶囊剂已于2018年11月获批临床,此次申报临床的是注射剂;氟唑帕利胶囊已于2019年10月申报上市,有望成为首个获批的国产PARP抑制剂,此次申报临床的或为新适应症;甲磺酸阿帕替尼片已于2014年10月获批上市,2018年在中国公立医疗机构终端销售额超过20亿元,此次为新适应症申报临床;醋酸阿比特龙片(I)为改良型新药,西安杨森的醋酸阿比特龙片在2018年在中国公立医疗机构终端销售额接近5亿元;注射用卡瑞利珠单抗是国内第3个获批上市的国产PD-1,此次为新适应症申报临床。
来源:米内网数据库、CDE等
注:数据统计于12月13-27日,按药品名称统计,不包含原料药、预防用生物制品等;申请类型不包含再注册、复审申请、技术转移、一次性进口等补充申请。