
精彩内容
日前,以“聚焦创新·共谋发展”为主题的新形势下医药企业创新论坛暨2019年广东省生物医药创新技术协会会员大会在广州举行。会上,广东东阳光药业有限公司研究院院长唐新发分享了东阳光药的创新与国际化之路。
东阳光药即将迎来收获期,公司将在2023年底前提交11个新药上市申请,其中7个新药有望在2023年底前获批上市;此外,预计在2023年底前,公司将有6个糖尿病生物药获批上市,仿制药获批上市数量有望超过100个(中国32,美国40,欧洲27)……
创新药大爆发!东阳光11款新药在路上
东阳光药未来上市新药
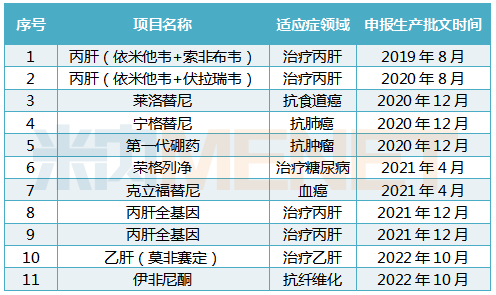
东阳光药在研新药涵盖抗感染领域、抗肿瘤领域、内分泌及代谢类疾病等治疗领域。11款在研新药中,抗丙型肝炎新药磷酸依米他韦已经获得国家药品监督管理局受理(受理号:CXHS1900030),并于今年11月8日获纳入优先审评。磷酸依米他韦是东阳光药自主研发的1类抗丙肝口服直接抗病毒药物(DAA),也是公司首个获得受理的国家1类新药,有望成为中国未来治疗丙肝病毒感染的重要产品。
公司预计到2023年将有4个抗丙肝新药上市。DAA是丙肝的主要治疗方法,近年来随着新药研发的突破性进展,丙肝已经可以通过DAA达到治愈。在中国大陆地区完成的II期及III期临床试验数据显示,磷酸依米他韦针对基因1型无肝硬化丙肝患者疗效显著,SVR12(12周持续病毒应答率)达99.8%,且用药安全性及耐受性良好。
抗乙肝新药甲磺酸莫非赛定是东阳光药First in class的一款重磅新药,数据显示,莫非赛定是所有疗法中已证实可明确抑制s抗原、e抗原的小分子化合物,可抑制cccDNA、是实现乙肝治愈不可或缺的靶点。
抗肿瘤领域,东阳光药以明显的临床获益为目标,专注于未满足临床需求的适应症,加快肿瘤靶向药研发进程。莱洛替尼用于治疗经二线治疗失败的食管癌患者、宁格替尼是可解决三代EGFR-TKI(表皮生长因子受体-酪氨酸激酶抑制剂)耐药的特效药,目前均尚无药物获批;克立福替尼用于治疗FLT3-ITD(Fms样酪氨酸激酶3-内部串联重复基因突变)突发的复发/难治AML(急性髓性白血病),疗效、安全性显著优于现有药物。
6大生物药将上市!糖尿病产品线全布局
米内网数据显示,2018年中国公立医疗机构终端糖尿病用药销售额为512.28亿元,同比增长12.79%。其中,非胰岛素类降血糖药占据49.47%的市场份额,胰岛素及其类似药占比45.41%,其他糖尿病用药占比5.12%。
2018年中国公立医疗机构终端糖尿病用药小类格局
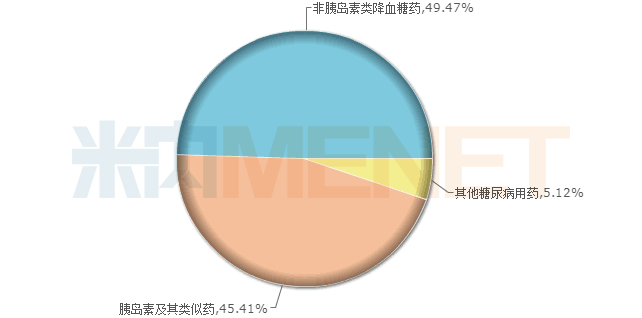
据国际糖尿病联盟糖尿病图谱数据,中国糖尿病患者目前居全球首位,且预计到2040年将达1.51亿,糖尿病用药在我国仍有潜在的巨大用药需求。针对糖尿病,东阳光药开辟仿创结合的研发策略,配合化学药系列,布局了全面的糖尿病产品线。
对于糖尿病生物类似药,东阳光药布局的二代胰岛素有重组人胰岛素(短效)、重组人胰岛素(预混30R);三代胰岛素有甘精胰岛素、门冬胰岛素、门冬胰岛素(预混30)、四代胰岛素有德谷胰岛素、德谷胰岛素+利拉鲁肽、德谷胰岛素+门冬胰岛素;GLP-1类似物则有利拉鲁肽、杜拉鲁肽等。
在糖尿病生物新药方面,东阳光药布局了GLP-1/FGF-21、GLP-1/GCG新结构生物药;创新剂型口服利拉鲁肽、口服胰岛素;以及SGLT2抑制剂新药荣格列净、DPP4系列仿制药化学药系列等。
其中,重组人胰岛素注射液、甘精胰岛素注射液、精蛋白重组人胰岛素注射液(预混30R)、门冬胰岛素注射液、门冬胰岛素30注射液、利拉鲁肽注射液等6个生物药是东阳光药计划在2023年底前上市的产品。
9个品种过评,芬多莫德美国首仿获批
米内网数据显示,截至目前,东阳光药通过或视同通过一致性评价品种已达9个。其中,有6个品种为首家过评,苯溴马隆片、磷酸奥司他韦胶囊、克拉霉素片、克拉霉素缓释片、左氧氟沙星片等5个品种目前仍为独家过评。东阳光药表示,未来两年内通过一致性评价的品种数将超过35个。
东阳光药通过一致性评价品种情况
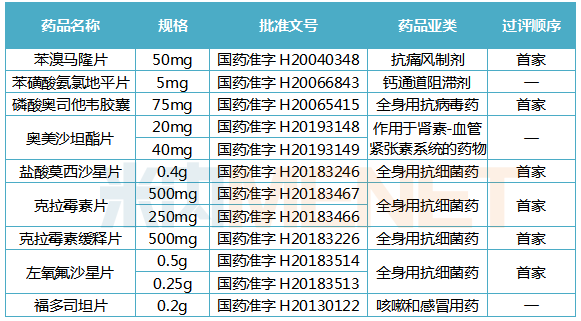
苯溴马隆为促进尿酸排泄类药物,通过抑制肾小管对尿酸的重吸收,从而降低血中尿酸浓度。苯溴马隆片(商品名:尔同舒)为东阳光药的重点产品之一,是临床治疗高尿酸血症的主要方案之一。米内网数据显示,2018年中国公立医疗机构终端抗痛风制剂销售额为16.39亿元,同比增长83.55%。东阳光药苯溴马隆片为目前国内过评的唯一一个降尿酸药。
磷酸奥司他韦胶囊是东阳光药的抗流感明星产品,目前国内独家通过一致性评价,磷酸奥司他韦颗粒一致性评价工作也在推进中。磷酸奥司他韦是一种神经氨酸酶抑制剂,是目前国际上预防和治疗流感的主选用药,也是现阶段治疗儿童流感安全有效性俱佳的药物;儿童适用的可威颗粒剂工艺,东阳光药拥有全球独家专利,还有11年的垄断保护期。据米内网数据,2018年中国公立医疗机构终端磷酸奥司他韦销售额为25.32亿元,同比增长68.71%。目前东阳光药可威胶囊和可威颗粒都已纳入2019版国家乙类医保药物目录,仍存在巨大的市场空间。
12月4日,美国FDA批准东阳光药的盐酸芬戈莫德胶囊上市,同时获批首仿的还有印度药企必奥康和太阳药业。芬戈莫德为神经鞘氨醇1-磷酸受体调节剂,是全球首个获批治疗多发性硬化症的口服药物。芬戈莫德原研药为诺华的捷灵亚,2018年全球销售额为33.41亿美元,2019年7月12日获批国内上市。
2015-2019H1东阳光药研发投入情况(单位:百万元)
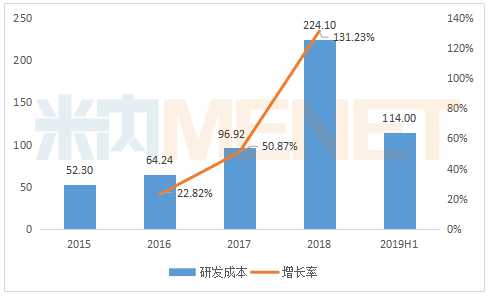
结语
近年来,东阳光药不断加大研发投入,2018年公司研发投入2.241亿元,同比增长131.23%,2019年上半年研发投入1.14亿元。可以看到,随着药品审评审批提速、带量采购不断推进、医保药品结构优化,创新药逐渐成为支撑我国医药市场发展的关键因素,国内主流药企转型创新的决心更加坚定、动作也更加迅速。
来源:米内网数据库