
摘要
11月CDE共承办药品注册申请897件
8个品种首次有企业申报一致性评价
5个1类新药申报上市
卡瑞利珠单抗有新适应症上市申请
仿制申请中有7个品种为首家仿制申报
贝达药业1类新药盐酸恩莎替尼胶囊获批
4个首仿品种获批
CDE总体承办情况
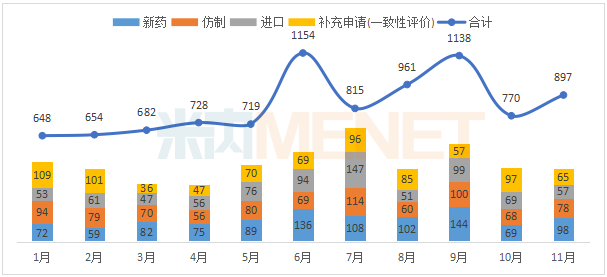
据MED中国药品审评数据库2.0统计,2020年11月CDE共承办药品注册申请897件。
2020年1-11月CDE承办药品注册申请情况(按受理号计)
一致性评价补充申请承办情况
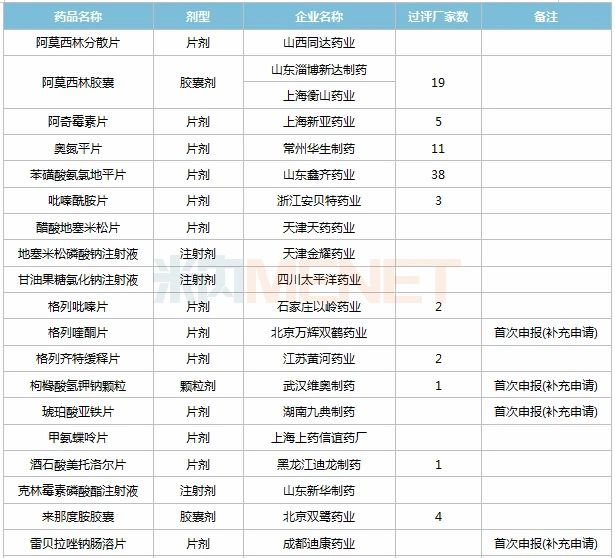
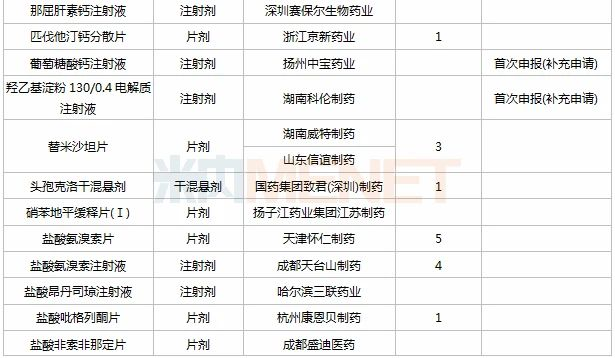
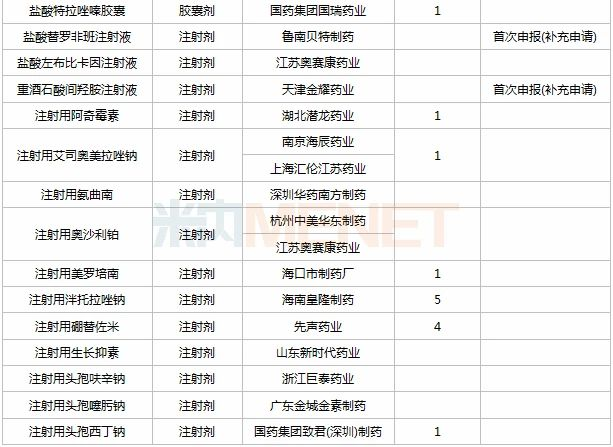
11月,46个品种的一致性评价补充申请获CDE承办。其中口服制剂品种有23个,注射剂品种有22个,格列喹酮片(北京万辉双鹤药业)、枸橼酸氢钾钠颗粒(武汉维奥制药)、琥珀酸亚铁片(湖南九典制药)、雷贝拉唑钠肠溶片(成都迪康药业)、葡萄糖酸钙注射液(扬州中宝药业)、羟乙基淀粉130/0.4电解质注射液(湖南科伦制药)、盐酸替罗非班注射液(鲁南贝特制药)、重酒石酸间羟胺注射液(天津金耀药业)等8个品种为首次一致性评价补充申请。详细情况见下表:
2020年11月CDE补充申请(一致性评价)品种承办情况
新药申请承办情况
11月,67个品种的新药申请获CDE承办,属于1类新药的有51个;2类改良型新药的有10个;此外还有4个3.3类生物类似药。南京圣和药业提交丙肝1类新药和乐布韦片上市申请,基石药业提交PD-L1单抗舒格利单抗注射液上市申请,苏州盛迪亚生物提交注射用卡瑞利珠单抗新适应症上市申请,详细情况见下表:
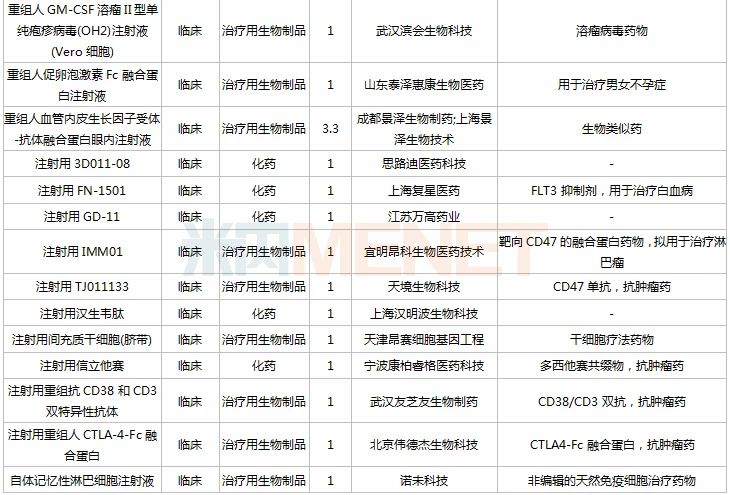
2020年11月国内新药上市申请承办情况
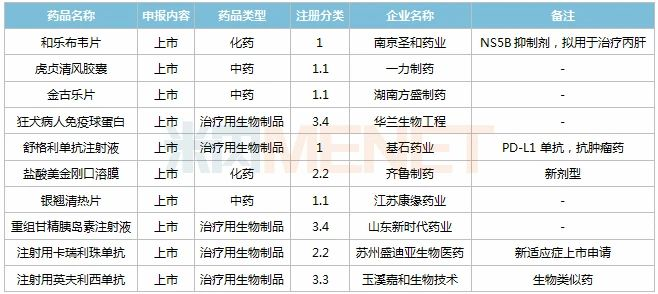
2020年11月国内新药临床申请承办情况
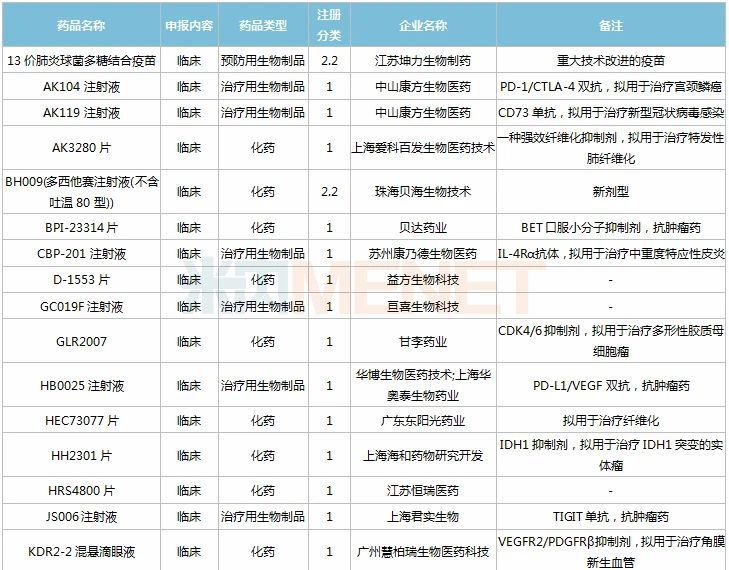
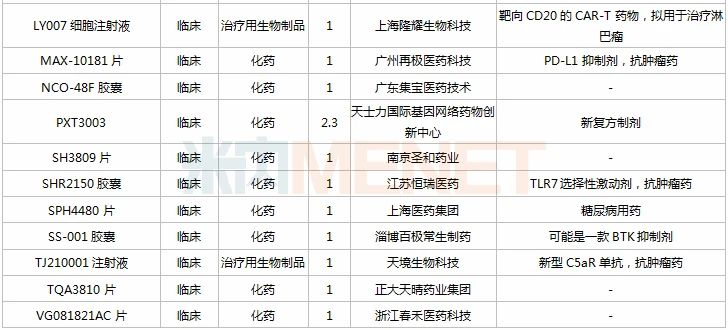
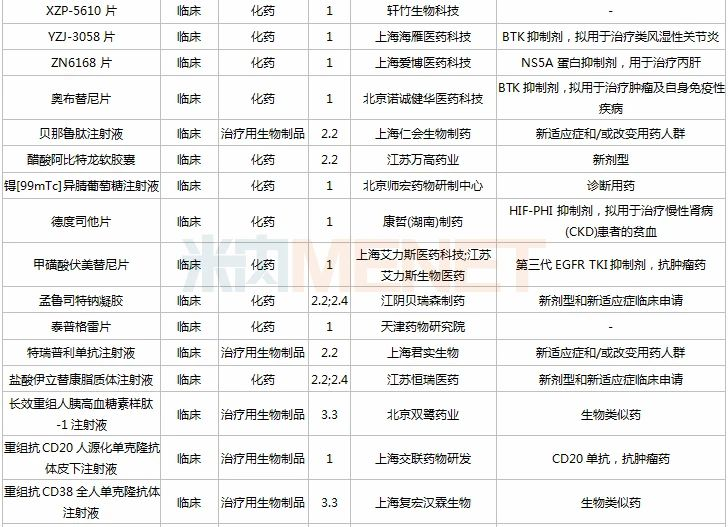
 仿制申请承办情况
仿制申请承办情况
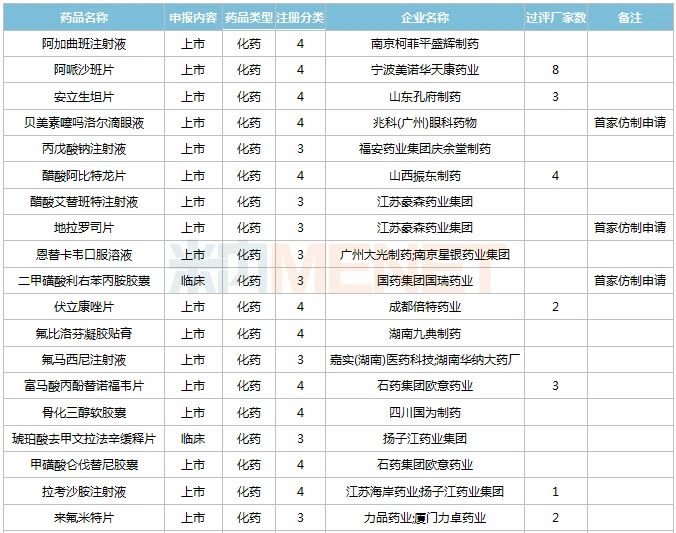
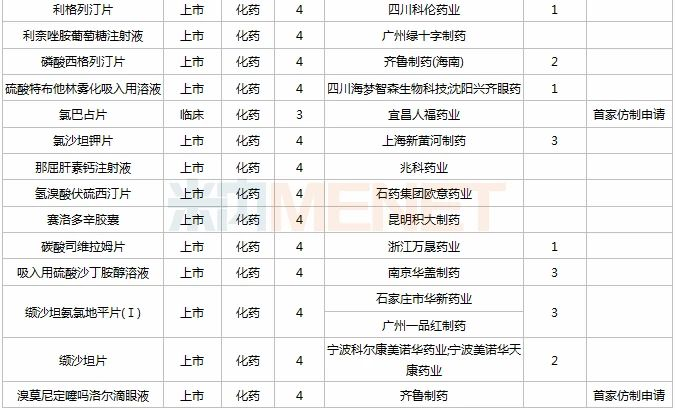
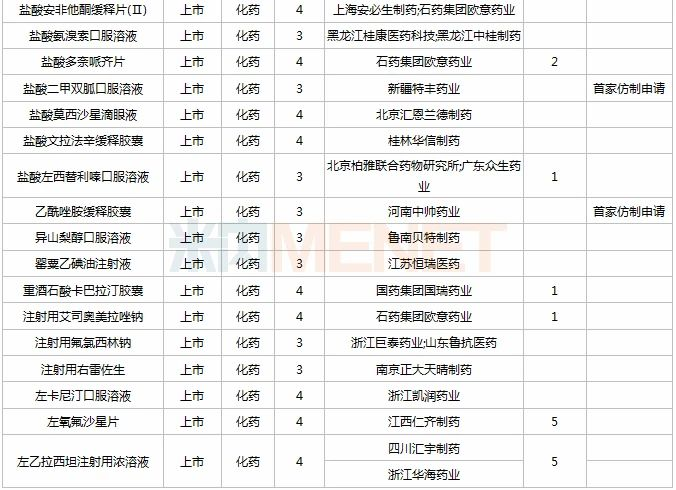
11月,50个品种的仿制申请获CDE承办,其中按3类申报的有17个,按4类申报的有33个;贝美素噻吗洛尔滴眼液(兆科(广州)眼科药物)、地拉罗司片(江苏豪森药业集团)、二甲磺酸利右苯丙胺胶囊(国药集团国瑞药业)、氯巴占片(宜昌人福药业)、溴莫尼定噻吗洛尔滴眼液(齐鲁制药)、盐酸二甲双胍口服溶液(新疆特丰药业)、乙酰唑胺缓释胶囊(河南中帅药业)等7个品种为首仿申请。详细情况见下表:
2020年11月国内仿制申请承办情况
进口申请承办情况
11月,42个品种的进口申请获CDE承办,其中1类新药有16个;2类改良型新药有9个,5.1类进口原研药9个,5.2类进口仿制药3个。详细情况见下表:
2020年11月进口上市申请承办情
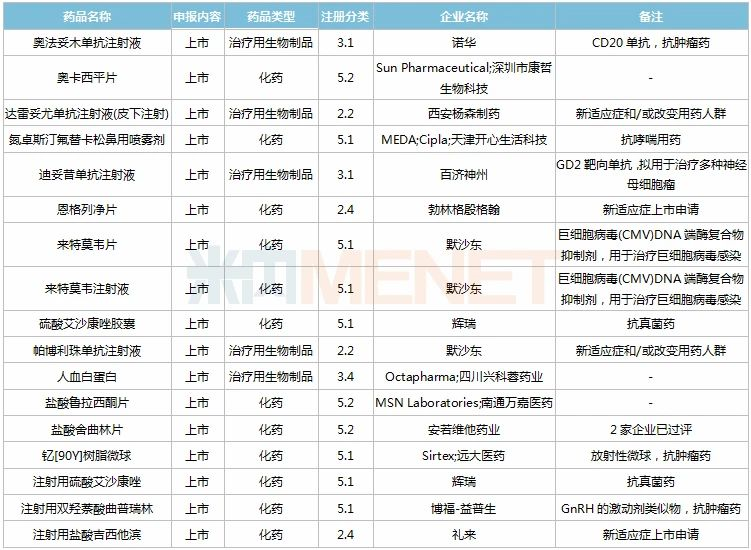 2020年11月进口临床申请承办情况
2020年11月进口临床申请承办情况
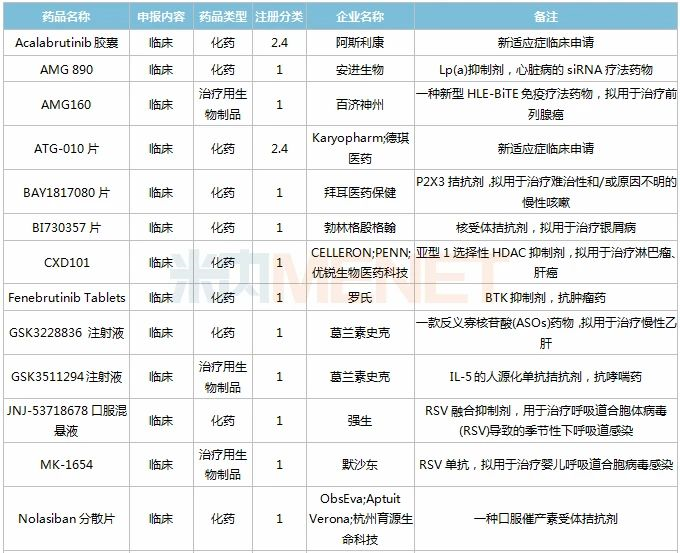
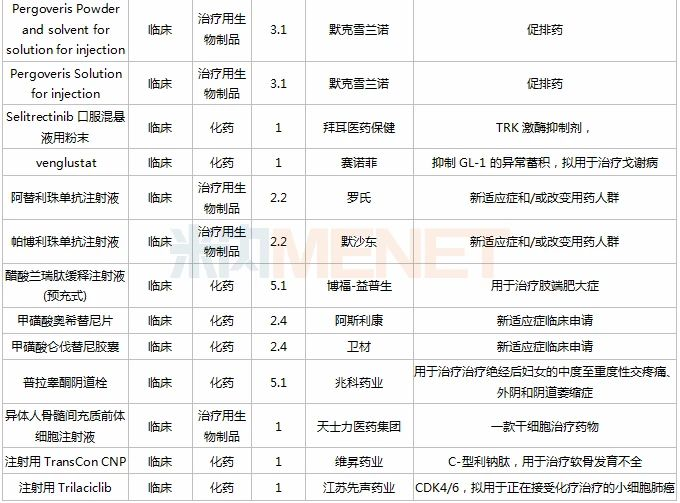
获批情况
据MED中国药品审评数据库2.0统计,11月有2个新药获批上市:贝达药业(盐酸恩莎替尼胶)、江苏豪森药业集团(奥氮平口腔速溶膜);50个仿制药获批(3类、4类、5.2类),其中泊马度胺胶囊(正大天晴药业集团)、恩替卡韦口服溶液(扬子江药业集团江苏制药)、拉考沙胺注射液(江西青峰药业)、盐酸美金刚缓释胶囊(成都苑东生物制药)等4个品种为首仿品种;详细情况见下表:
2020年11月部分品种获批情况
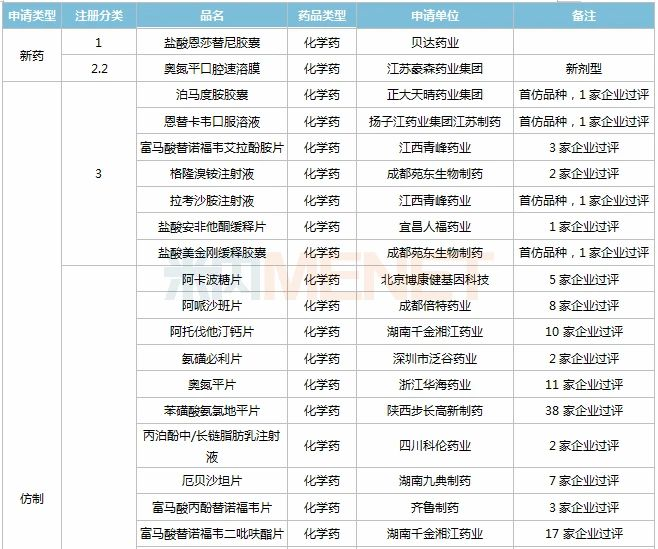
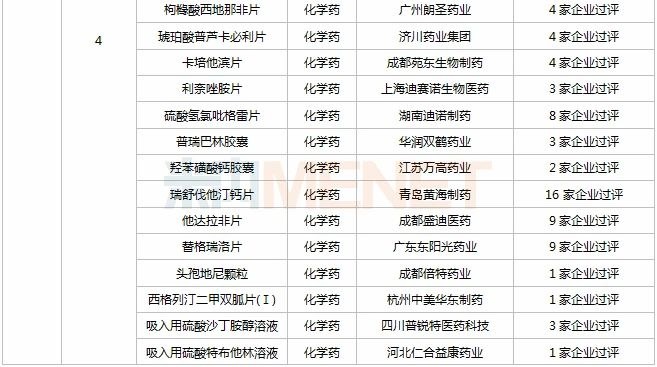
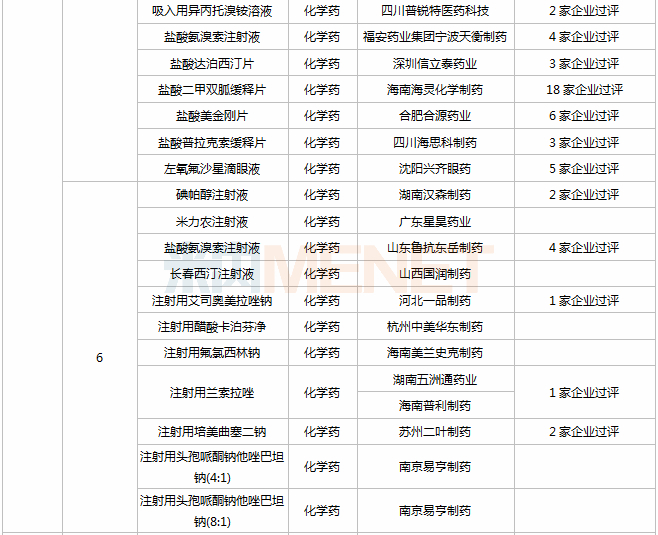
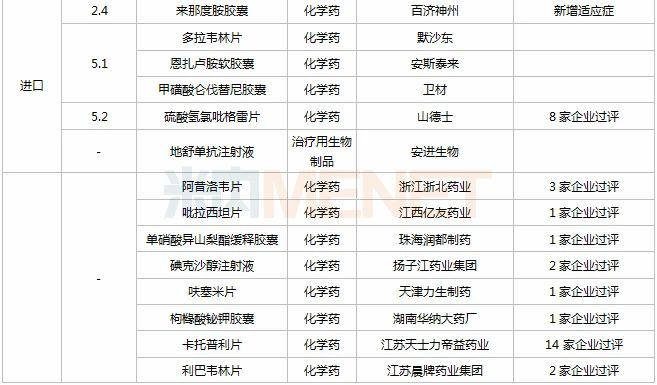
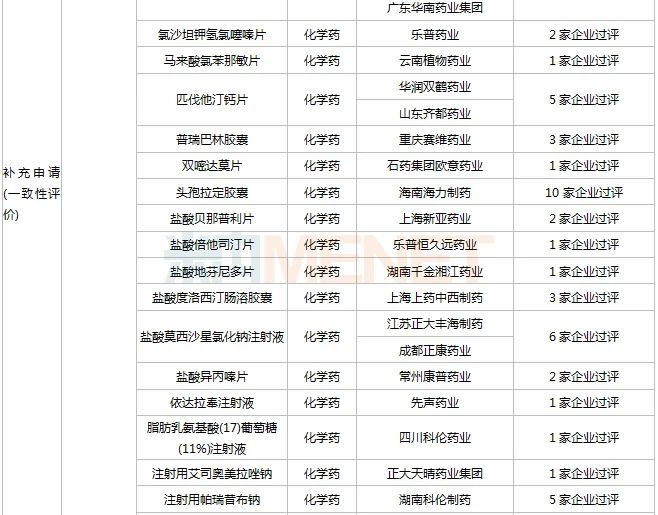
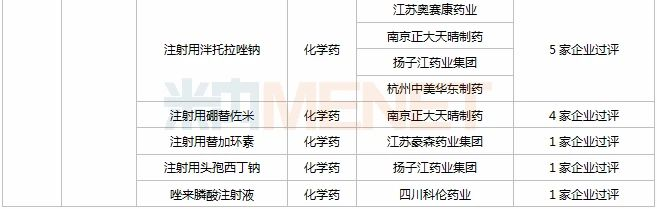
数据来源:米内网MED药品审评数据库2.0、CDE、NMPA;过评数统计截至2020年12月4日,相关统计字段按药品名称统计;药物作用靶点以及适应症来自公开资料,如有疏漏,欢迎指正。